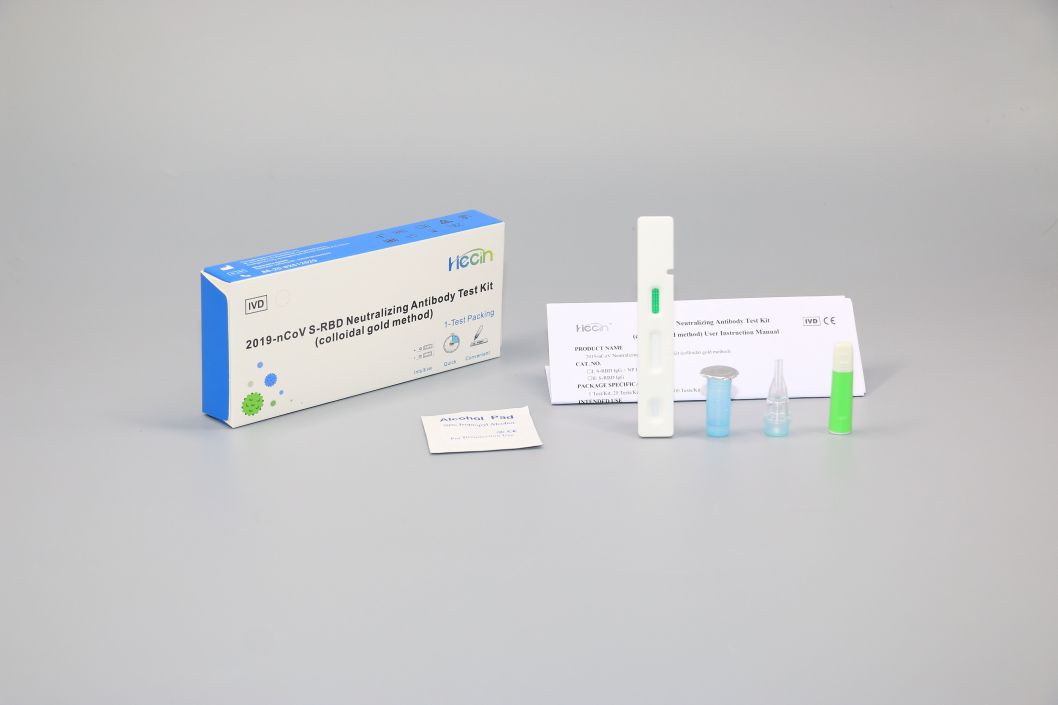
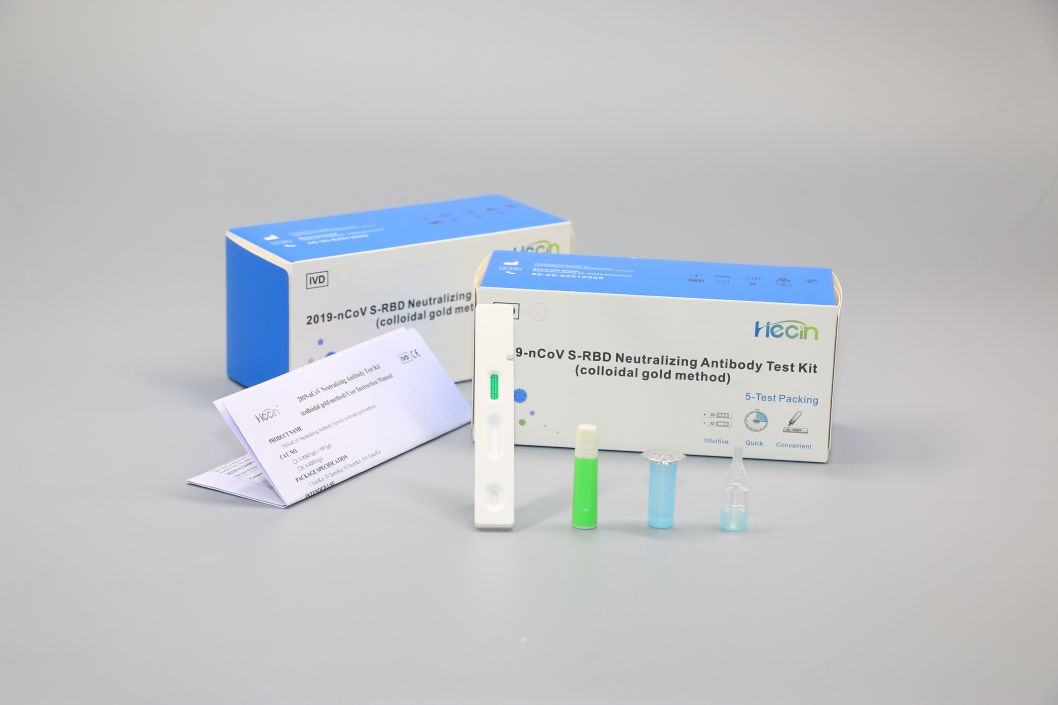
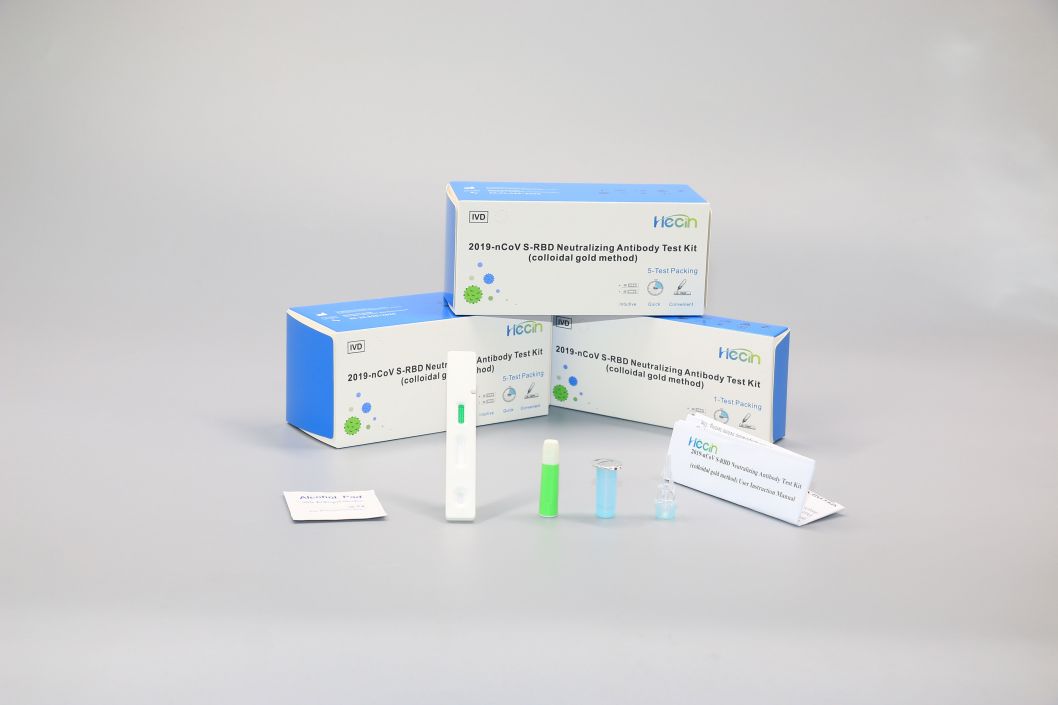
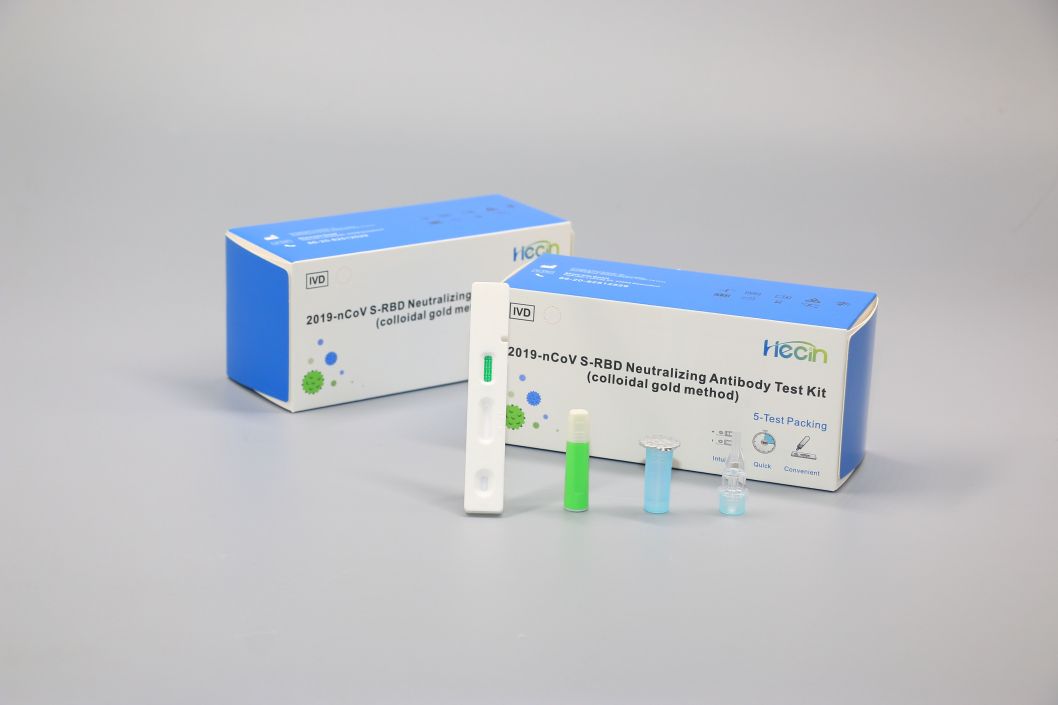
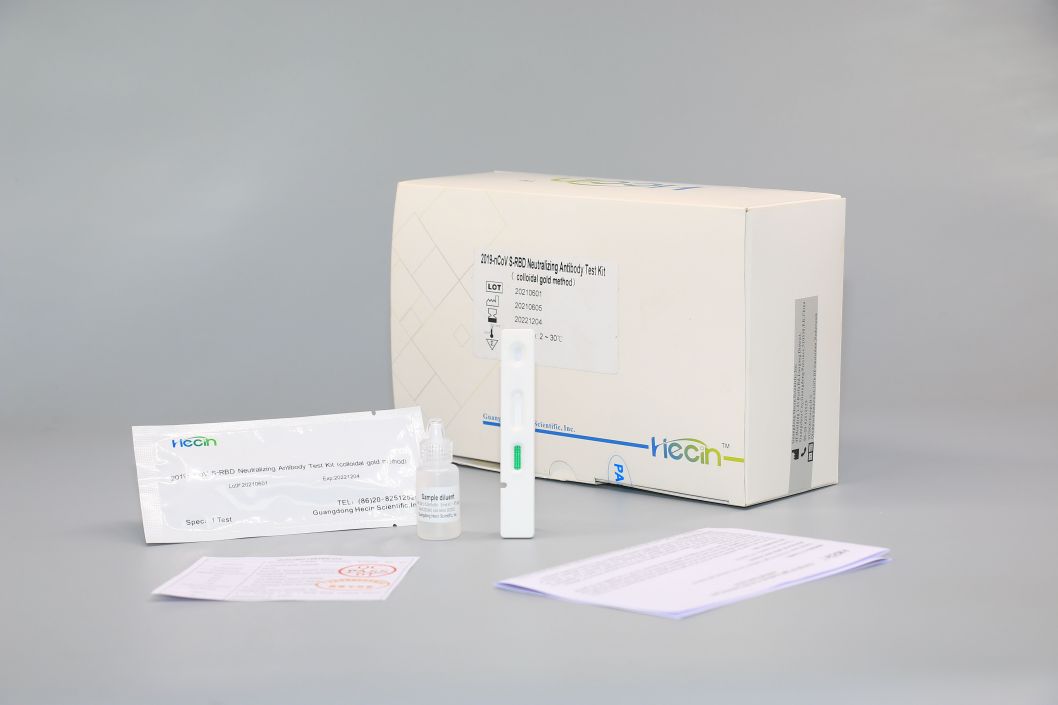
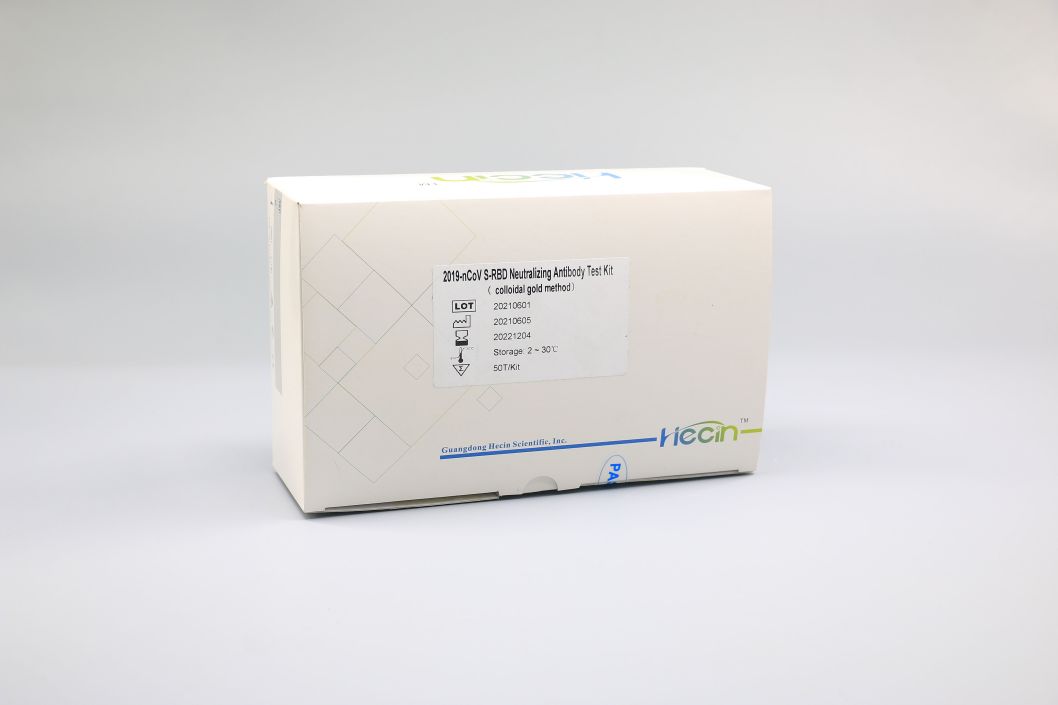
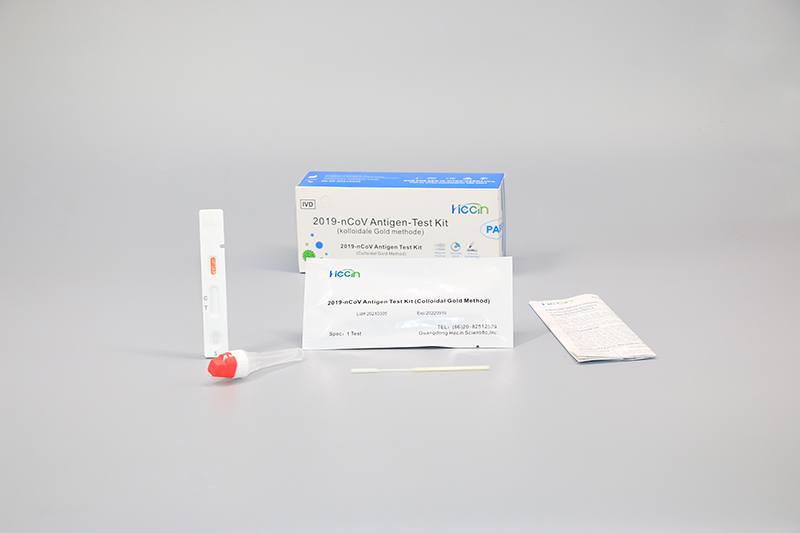
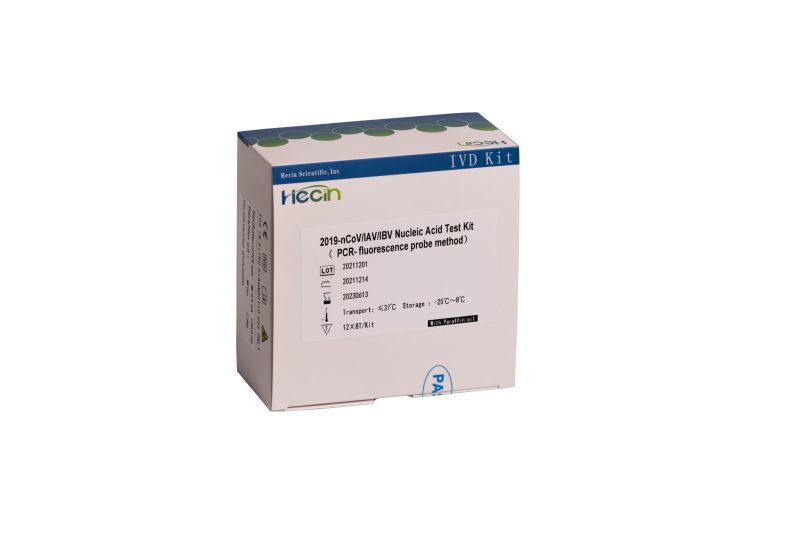
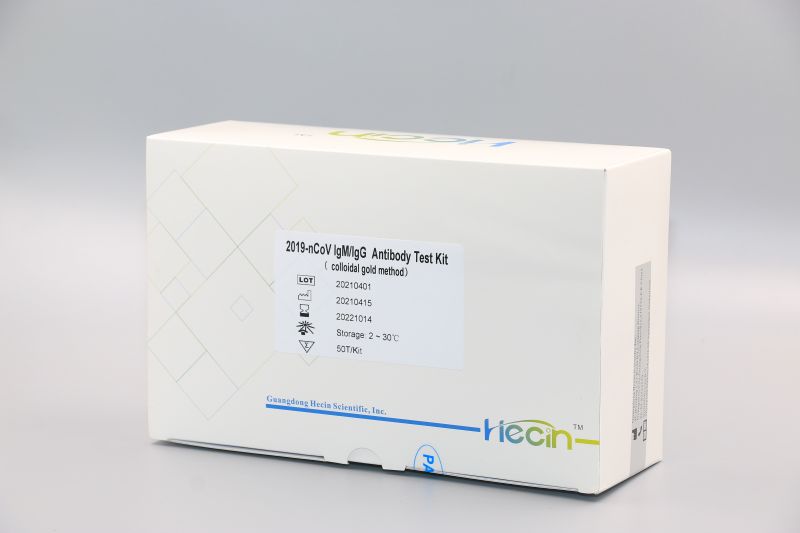
Testkit für neutralisierende Antikörper 2019-nCoV S-RBD (Kolloidalgold-Methode)
Einführung
Derzeit werden alle in der klinischen Entwicklung befindlichen 2019-nCoV-Impfstoffkandidaten durch intramuskuläre Injektion verabreicht.Eine intramuskuläre oder intradermale Impfung kann zu einer starken Induktion von Serum-IgG führen
Derzeit werden mehr als 180 Impfstoffkandidaten gegen 2019-nCoV entwickelt, die auf verschiedenen Plattformen basieren.
Das S-Protein ist das Hauptziel neutralisierender Antikörper;
Viele dieser neutralisierenden Antikörper zielen auf die RBD des S-Proteins ab.
Wie beurteilt man die Wirksamkeit des 2019-nCoV-Impfstoffs? --- Testkit für neutralisierende Antikörper
Vorteil
Tests vor der Impfung
Vor der Impfung können die Kandidaten den neutralisierenden Antikörper von RBD nachweisen, um festzustellen, ob eine Impfung erforderlich ist;
Die meisten Impfungen sind abgedeckt
Es kann neutralisierende Antikörper nachweisen, die von den meisten Impfstoffen auf dem Markt produziert werden;
Schnell und bequem
Die Bedienung ist einfach, es ist keine Geräteerkennung erforderlich, die Ergebnisse können innerhalb von 15 Minuten erhalten werden.
Identifikationsfunktion
Es kann den neutralisierenden Antikörper von 2019-nCoV, der durch den 2019-nCoV-Impfstoff produziert wird, oder den Antikörper, der durch die 2019-nCoV-Infektion für eine bestimmte Art von Impfstoffen produziert wird, wie z. B. einen viralen Vektorimpfstoff (nicht replizierend), einen RNA-Basisimpfstoff und einen Proteinuntereinheitenimpfstoff, unterscheiden ;
Vollbluttest
Der Vollbluttest macht die Operation komfortabler;
Geltungsbereich
Vor der Impfung
Stellen Sie fest, ob sie sich mit dem neuen Coronavirus infiziert haben und ob sie noch geimpft werden müssen;
Impfzeitraum
Bestimmen Sie, ob wirksame neue neutralisierende Antikörper produziert werden;
Spätes Impfstadium
Je nach Epidemiegebiet von 2019-nCoV wird empfohlen, regelmäßig alle drei Monate das Vorhandensein neutralisierender 2019-nCoV-Antikörper nachzuweisen.
Komponenten
| Komponenten | Hauptzutaten | Lademenge (Spezifikation) | ||
| 1 T/Kit | 20 T/Satz | 50 T/Satz | ||
| Testkarte | Teststreifen mit kolloidalem Gold markiertem Anti-Human-IgG-Antikörper, kolloidalem Gold markiertem Anti-Huhn-IgY-Antikörper, rekombinantem 2019-nCoV S-RBD-Protein und Hühner-IgY-Antikörper | 1 Stk | 20 Stk | 50 Stück |
| Probenverdünnungsmittel | 0,01 M Phosphatpufferlösung, 0,5 % Tween-20 | 0,5 ml | 5 ml | 10 ml |
Leistung
| Hecin-Reagenz | Klinischer Serumvirus-Neutralisationstest | Gesamt | |
| Positiv | Negativ | ||
| Positiv | Positiv | 84 | 9 |
| Negativ | Negativ | 8 | 198 |
| Gesamt | Gesamt | 92 | 207 |
| Klinische Empfindlichkeit | Klinische Empfindlichkeit | 84/92 91,30 % (95 % KI: 83,58 %~96,17%) | |
| Klinische Spezifität | Klinische Spezifität | 198/207 95,65 % (95 % KI: 91,91 %~97,99%) | |
| Genauigkeit | Genauigkeit | 282/299 94,31 % (95 % KI: 91,05 %~96,65%) | |
Leistung des Hecin-Reagenzes im Vergleich zur Vergleichsmethode bei Serum-/Plasmaproben.
| Hecin-Reagenz | Klinischer Serumvirus-Neutralisationstest | Gesamt | |
| Positiv | Negativ | ||
| Positiv | 84 | 8 | 92 |
| Negativ | 8 | 199 | 207 |
| Gesamt | 92 | 207 | 299 |
| Klinische Empfindlichkeit | 84/92 91,30 % (95 % KI: 83,58 %~96,17%) | ||
| Klinische Spezifität | 199/207 96,14 % (95 % KI: 92,53 %~98,32%) | ||
| Genauigkeit | 283/299 94,65 % (95 % KI: 91,46 %~96,91%) | ||
Leistung des Hecinreagenzes im Vergleich zur Vergleichsmethode bei Vollblutproben.
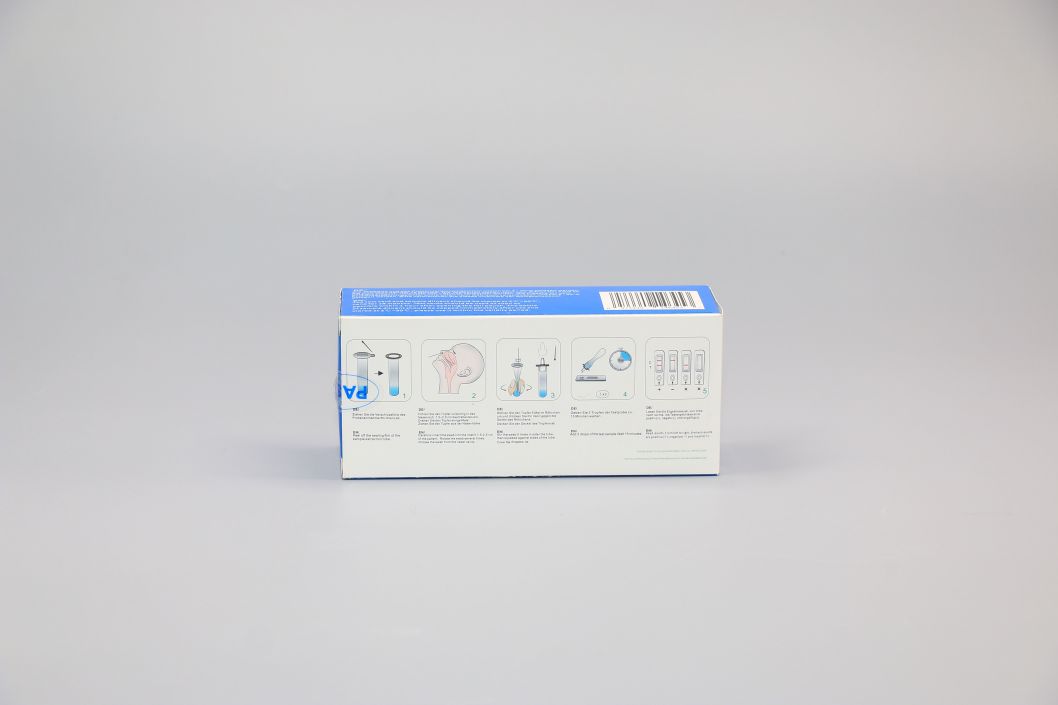
Testprozedur
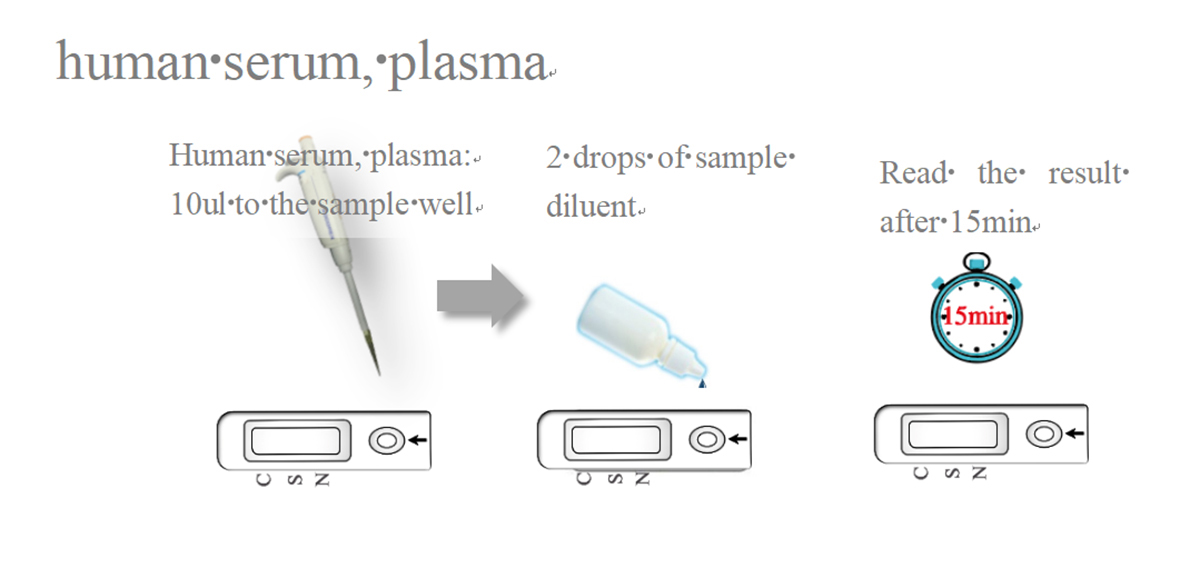
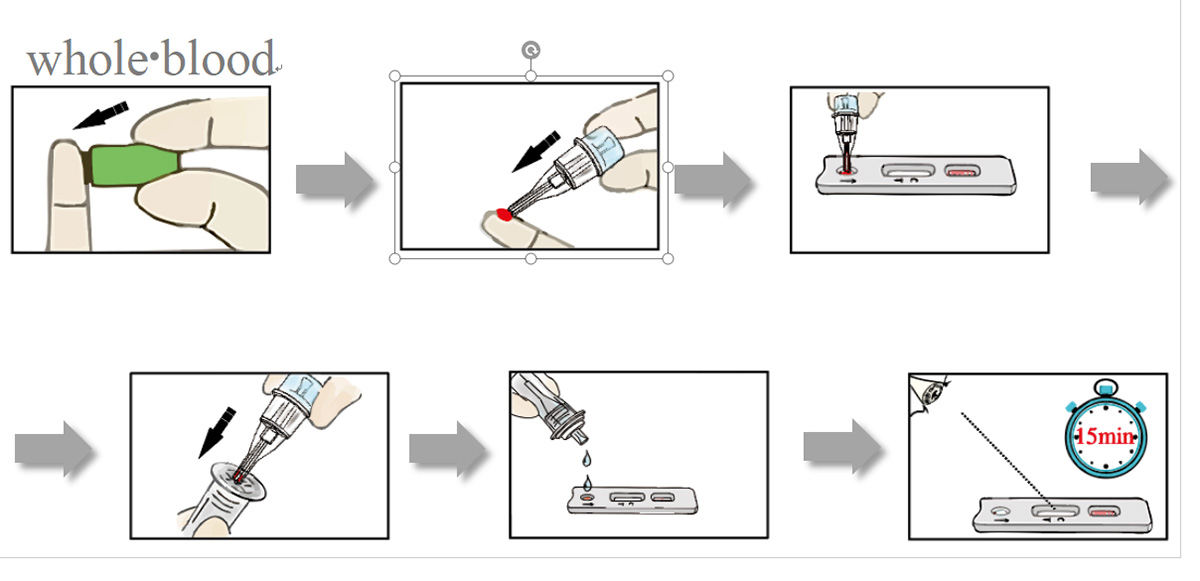
Registrierungs-Zertifikat



JT08-1T
JT08-5T
JT08-50T